EY新日本有限責任監査法人 ライフサイエンスセクター
公認会計士 西川 太一/黒田 剛史
1. CMO・CDMOの概要
(1) CMO
CMOとは、Contract Manufacturing Organizationの略称で、医薬品製造受託企業を指します。CMOは製薬企業から医薬品の製造を受託し、受託料をもらうことを事業にしている企業です。以前から存在していた事業でしたが、日本では、2005年4月施行の改正薬事法(現:薬機法)により、医薬品製造の全面的な外部委託が可能となったことで、CMO市場が大きく拡大し、存在が非常に大きなものとなりました。
製薬企業において創薬から新薬の製造・販売まで、大規模な投資が必要となることから、近年、製薬企業は研究開発部分に経営資源を集中させるために、医薬品製造についてはCMOに委託するケースが多くあります。これを「水平分業」といい、このあと記述するCDMOやCRO(医薬品開発業務受託企業)と並んで、現在の製薬企業において経営を効率化するために重要度が増しています。
また、特許権の切れている新薬である長期収載品についても経営の効率化の観点からCMOに製造委託するケース、ジェネリック医薬品について設備投資の効率化により製造をCMOに委託するケースもあります。このように、CMOのニーズは様々で、市場規模は年々増加している状況にあります。
(2) CDMO
CDMOとは、Contract Development and Manufacturing Organizationの略称で、上記CMOが担う製造に加えて、製剤研究や治験薬製造などを含む開発業務を受託する企業のことを指します。製薬企業において創薬部分に経営リソースを集中させ、量産するための開発の部分をCDMOに委託し、さらなる経営の効率化を図るニーズがあり、拡大が続いている領域です。
バイオ医薬品については特にニーズが高まっています。バイオ医薬品の製造は膨大な初期投資と特別な技術・ノウハウが必要となるため、外部リソースであるCDMOを活用しようとする動きがより活発です。バイオ医薬品が医薬品市場に占める割合は上昇傾向にあり、それに伴いバイオ医薬品のCDMO市場も成長を続けています。
当該CDMOの国内の直近の動向としては、医薬品業界以外からの企業の参入が多いことがあげられます。直近では、富士フィルム、旭化成、AGCなどM&Aや積極的な設備投資でグローバルに活躍するCDMOも増えています。
2. 会計処理の特徴
(1) 棚卸資産・売上原価に係る特徴
製品の受注・販売取引に関して、CMO・CDMOでは次のような特徴があります。
a. 原価計算の方法
医薬品の製造においては、GMP(Good Manufacturing Practice)という医薬品の製造管理及び品質管理に関する基準に準拠することが求められます。「日本医薬品原薬工業会」によると、GMPを理解するうえで重要な考え方として「GMPの三原則」があり、日本のGMPをはじめ、諸外国のGMPも以下の要件にまとめられているとされています。
- 人為的な誤りを最小限にすること
- 医薬品の汚染及び品質低下を防止すること
- 高い品質を保証するシステムを設計すること
他業種と異なり、医薬品製造を行うCMOでは、GMPに準拠し生産を実施する必要があり、工程管理や衛生管理の手順が厳格に管理されることから高品質で安定的な生産が可能であると考えられます。作業が明確となっているため、一般的に、棚卸資産価額及び売上原価算定のための個々の適切な標準原価の設定が可能である場合が多いと考えられます。
なお、CMOでは、様々な得意先から多品種に渡る製造を受託するため、個別の受注内容に応じた製造設備の利用が考えられます。そのため、製造直接費のみならず、製造間接費の適切な管理も重要であると考えられます。
これらを踏まえ、CMOでは、標準原価計算制度を適用している場合が多いと考えられます。
さらに、筆者個人の経験によれば、CMOでは組別工程別総合原価計算を採用している場合が多く、加えて、標準原価計算で発生する原価差額は他業種と比べて小さくなる傾向にあると考えています。
CDMOの場合においても、標準原価計算制度を適用している場合が多いという点はCMOの場合と同様であると考えられます。加えて、CDMOは、得意先の開発の一部を受託すると、当該研究開発費を売上原価の一部として識別する必要があると考えられます。その一方で、自社のための研究開発も同時に行っている場合があり、それらは販売費及び一般管理費として識別されるため、発生した研究開発費が自社のためか受託務のためかの区別重要になると考えられます。
b. 棚卸資産の評価
CMOは委託元からの受注に基づき医薬品を生産しており、受託生産した品目について委託元以外へ販売することは想定していない場合が通常と考えられます。そのため、受託生産した在庫については、薬価や仕切価格の下落が生じたとしても、契約に基づき委託元へ販売・請求をすることができ、棚卸資産の正味売却価額の下落はないとして、帳簿価額の切下げは不要と判断する場合もあると考えられます。
また、当初契約締結の前提となる受注予定数量に対して、実際の受注数量と大幅な乖離がある場合も生じ得ます。このような場合に備え、当初契約の段階で、受注数量が少ない場合には受注単価が高くなるような変動対価を設定している場合もあります。加えて、委託元との交渉に基づき一時金を受領する場合もあると考えられます。
(会計処理)
薬価や仕切価格の下落が生じたとしても、契約に基づき委託元へ販売請求することができる場合、棚卸資産の帳簿価額の切下げは不要となる場合があります。
(2) 売上に係る特徴
a. 受注数量と出荷数量
医薬品業界では、バッチ生産が一般的な製造方法です。バッチ生産は、生産設備毎のサイズに応じた生産ができ受注数量に応じた生産設備の選定を行うことが可能であること、生産に要する時間が計画しやすく生産完了後は計画的に別の品種の生産を行うことができることといった特徴を有しています。加えて、バッチ毎の品質管理を行いやすいという特徴から、多品種の生産を実施することが想定されるCMOにおいても同様に一般的な製造方法として考えられます。
しかし、生産の都度、収率がわずかに異なるなどの理由から、受注数量に対して生産数量が若干前後することが生じます。仮に、正確に受注数量どおりの納品を行うことが必要であるとすると、生産数量が受注数量に対して少ない場合には、少量の納品のため追加で他に転用できない在庫を多く生産する必要が生じ、生産数量が受注数量に対して多い場合には、CMOでは生産した在庫の使途がなく有効活用することができないことなどの課題が生じます。
これらの点などを考慮して、CMOの受注数量に対して合理的な水準の変動の出荷数量であれば、発注元は全量を買い取り注残も残らないということが、業界の慣行となっていると考えられます。
(会計処理)
CMOにおいて、受注単価500/gの医薬品の製造1,000gを受注し、実際には生産数量1,010gを納品した場合を例にします。
【仕訳例】
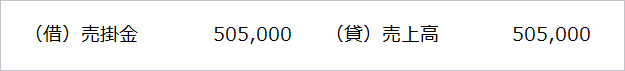
なお、収益の認識時点は、「収益認識に関する会計基準」に従うこととなり、CMOでは、通常、受託した医薬品を顧客に引渡した時点などになると考えられます。
b. CDMOにおける受託開発
CDMOでは、CMOのビジネスに加え、医薬品の製造方法の開発や、研究開発段階の治験薬の製造、製剤化検討、分析手法の検討及び関連する分析業務の実施など、多岐に渡る開発業務を受託しています。
収益の認識時点は、「収益認識に関する会計基準」に従い収益を計上することとなりますが、例えば、治験薬の製造であれば治験薬の納品時や開発の進捗に応じた役務提供の時などに、製造方法の開発や分析手法の開発であれば開発が完了し報告書を納品した時や役務提供や開発の進捗に応じて収益を認識することが考えられます。
参考文献・参考ウェブページ
日本医薬品原薬工業会「GMPとは - 日本医薬品原薬工業会」、jbpma.gr.jp/(2024年2月19日アクセス)
ライフサイエンス
- 第1回:ライフサイエンス業界の概要と動向(上) (2024.03.05)
- 第2回:ライフサイエンス業界の概要と動向(下) (2024.03.06)
- 第3回:新薬を中心とした医療用医薬品製造販売業の概要と会計処理の特徴 (2024.03.08)
- 第4回:一般用医薬品製造販売業の概要と会計処理の特徴 (2024.03.11)
- 第5回:ジェネリック医薬品(後発医薬品)を中心とした医療用医薬品製造販売業の概要と会計処理の特徴 (2024.03.13)
- 第6回:医薬品製造受託機関(CMO)・医薬品開発製造受託機関(CDMO)の概要と会計処理の特徴 (2024.03.14)
- 第7回:医療機器製造販売業の概要と会計処理の特徴 (2024.03.15)
- 第8回:医薬品卸売業の概要と会計処理の特徴 (2024.03.18)
- 第9回:バイオベンチャー企業のビジネスと財務諸表の特徴 (2024.03.25)
- 第10回:バイオベンチャー企業におけるライセンス契約の会計処理論点 (2024.03.26)
- 第11回:ライフサイエンス関連企業における不正・コンプライアンスリスクと最近の動向 (2024.03.27)
- 第12回:バイオベンチャー企業の株式上場における論点 (2024.03.28)
- 第13回:ライフサイエンス関連企業のサステナビリティ情報開示 (2024.04.02)




