EY新日本有限責任監査法人 ライフサイエンスセクター
公認会計士 冨田 哲也/小山 晃平
永岡 明典/松原 匠作
1. はじめに
ライフサイエンス、つまり生命科学とは、生物や人間の生命現象に関する科学の全般を指す広範囲な分野を意味する広い概念です。
これには、人々の健康や環境、生活の質の向上に貢献する様々な製品やサービスが含まれますが、私たちの健康に直結する観点では、医療の提供、予防医学、健康増進、リハビリテーション、患者のケアなど、直接的な治療や健康維持の実施に関わる広範な活動全体を指すヘルスケアと、ヘルスケアの背後にある医薬品や医療機器の科学的研究と技術開発を担当する狭義のライフサイエンスに分類することができます。
すなわち、医薬品や医療機器の開発といったライフサイエンスの成果は、ヘルスケアの一部として実施され、人々の健康に貢献するという関係性にあります。
本稿では、この狭義のライフサイエンス、つまり医薬品と医療機器に焦点を当てて、業界の概要やトレンドについて概説したのち、下記に示している主要な業態ごとに業界の特色や関連する会計処理、論点を後続のシリーズで解説します。
- 新薬
- 一般用医薬品(OTC)
- ジェネリック・後発薬
- CMO(CDMO)
- 医療機器
- 医薬品卸
- バイオベンチャー
また、上記のほかに、ライフサイエンス関連企業に関わる下記の領域についても、参考となる情報を解説します。
- Forensics
- IPO
- サステナビリティ(非財務情報)
2. 業界の特徴
(1) 医薬品及び医療機器業界を取り巻く規制
まず、ライフサイエンス業界のうち、特に医薬品及び医療機器が属する業界(以下、「医薬品業界」)の特徴として、政府の管理下にある規制産業であることがあげられます。ここでは、医薬品業界を取り巻く規制について説明します。
医薬品や医療機器は、人体の生命・健康そのものに影響を与えるものであるため、その有効性・安全性を確保するための様々な制度が存在しています。
日本では、厚生労働省が中心となり、医薬品を監督するための様々な規制を行っています。まず、法律として、医薬品等の有効性・安全性を確保するため、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(以下、「薬機法」)」に基づき、医薬品等の製造から販売、市販後の安全対策まで一貫した規制をかけています。
ここで薬機法の対象となっている医薬品等は、医薬品、医薬部外品、化粧品、医療機器及び再生医療等製品の5つを指します。それぞれの定義については以下の表の通りです。
図表1【医薬品等の定義】医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律 第2条(定義)より抜粋
| 区分 |
定義 |
| 1項 医薬品 | 一 日本薬局方に収められている物 二 人又は動物の疾病の診断、治療又は予防に使用されることが目的とされている物であって、機械器具等(機械器具、歯科材料、医療用品、衛生用品並びにプログラム(電子計算機に対する指令であって、一の結果を得ることができるように組み合わされたものをいう。以下同じ。)及びこれを記録した記録媒体をいう。以下同じ。)でないもの(医薬部外品及び再生医療等製品を除く。) 三 人又は動物の身体の構造又は機能に影響を及ぼすことが目的とされている物であって、機械器具等でないもの(医薬部外品、化粧品及び再生医療等製品を除く。) |
| 2項 医薬部外品 | 一 次のイからハまでに掲げる目的のために使用される物(これらの使用目的のほかに、併せて前項第二号又は第三号に規定する目的のために使用される物を除く。)であつて機械器具等でないもの イ 吐きけその他の不快感又は口臭若しくは体臭の防止 ロ あせも、ただれ等の防止 ハ 脱毛の防止、育毛又は除毛 二 人又は動物の保健のためにするねずみ、はえ、蚊、のみその他これらに類する生物の防除の目的のために使用される物(この使用目的のほかに、併せて前項第二号又は第三号に規定する目的のために使用される物を除く。)であつて機械器具等でないもの 三 前項第二号又は第三号に規定する目的のために使用される物(前二号に掲げる物を除く。)のうち、厚生労働大臣が指定するもの |
| 3項 化粧品 | 人の身体を清潔にし、美化し、魅力を増し、容貌を変え、又は皮膚若しくは毛髪を健やかに保つために、身体に塗擦、散布その他これらに類似する方法で使用されることが目的とされている物で、人体に対する作用が緩和なものをいう。ただし、これらの使用目的のほかに、第一項第二号又は第三号に規定する用途に使用されることも併せて目的とされている物及び医薬部外品を除く。 |
| 4項 医療機器 | 人若しくは動物の疾病の診断、治療若しくは予防に使用されること、又は人若しくは動物の身体の構造若しくは機能に影響を及ぼすことが目的とされている機械器具等(再生医療等製品を除く。)であつて、政令で定めるものをいう。 |
| 9項 再生医療等製品 | 一 次に掲げる医療又は獣医療に使用されることが目的とされている物のうち、人又は動物の細胞に培養その他の加工を施したもの イ 人又は動物の身体の構造又は機能の再建、修復又は形成 ロ 人又は動物の疾病の治療又は予防 二 人又は動物の疾病の治療に使用されることが目的とされている物のうち、人又は動物の細胞に導入され、これらの体内で発現する遺伝子を含有させたもの |
これらの医薬品等の定義にあてはまる製品を製造・販売する事業者については、薬機法に従い、品質、有効性及び安全性を確保することが求められます。
また、薬機法においては、薬局の開設に関する都道府県知事の許認可、医薬品等の製造・販売に関する厚生労働大臣による許認可の規定が存在しています。これらの許認可を維持するために企業は薬機法に定められた様々なルールを遵守しなければなりません。さらに、厚生労働省又は都道府県は、事業者の事業所に立入検査を行い、品質・安全管理基準に適合していない事項があった場合には、改善命令等として一定期間の業務停止命令を発することができます。また違反の度合いに応じて、許可の取消しや承認の取消しをすることもできます。
さらに医薬品、医薬部外品、一部の化粧品及び医療機器の製造販売にあたっては、品目ごとにその製造販売について厚生労働大臣の承認を受ける必要があります。申請にあたっては、臨床試験の試験成績に関する資料等を添付して申請を行い、製品の品質、有効性及び安全性に関する審査を受ける必要があります。
これらのことから、医薬品業界は政府により製品の製造販売が管理されている規制産業であるといえます。
また、医薬品等の品質、有効性、安全性を担保するための機関として、厚生労働省所管の独立行政法人医薬品医療機器総合機構(以下、「PMDA」)が存在しています。
PMDAは医薬品の副作用の被害者を救済するための機関でしたが、現在は、規制当局として、健康被害救済、医薬品や医療機器などの承認審査、安全性に関する情報の収集、分析、提供といった業務を実施しています。PMDAは、その業務の一部として、医薬品等の製造販売に関する審査や、医薬品等製造事業者の基準適合性調査業務なども請け負っています。またPMDAは、ホームページにおいて医薬品・医療用機器等の安全性情報・回収情報といった様々な情報発信を行っています。
次に、海外に目を向けます。
米国ではThe Food and Drug Administration(以下、「FDA」)が医薬品等の安全性及び有効性を確保するための機関として存在しています。FDAでは、医薬品等の審査や承認、臨床試験の規制、薬価の管理、医薬品の製造販売事業者に対する品質・安全管理のモニタリング、市場への情報提供といった業務を実施しています。またFDAでは、それ以外にも、未成年者による喫煙を減らすための活動や、国内の食料供給、放射線を発生させる製品の安全性確保などの業務も実施しています。
EUでは、European Medicines Agency(以下、「EMA」)という組織が存在しており、この組織が医薬品等の審査や承認、臨床試験の規制、医薬品の製造販売事業者に対する品質、安全管理のモニタリングといった活動を実施しています。EMAで評価された医薬品についてはEU圏内で有効な承認を受けます。なお、EMAは薬価の設定には関与しません。
これ以外にも、イギリスでは、Medicines and Healthcare products Regulatory Agency(MHRA)、中国では国家薬品監督管理局(NMPA)といった機関が医薬品の承認、医薬品の安全性、品質、有効性の評価を行っています。
このように、医薬品等の製造販売については地域別に規制当局が存在しており、国によって規制が異なります。そのため、自国で開発した医薬品等を他国で販売する際には、各地域の規制当局において、改めて製造販売承認を受けなければならない点も特徴です。他国で承認されている医薬品が自国で承認されず利用できない状況は「ドラッグ・ラグ」と呼ばれています。
(2) 市場環境
次に、医薬品業界の市場環境について、解説します。
まず、市場規模ですが、2022年度の世界の医療用医薬品市場の規模は約1兆1390億米ドル(1米ドル=140円換算で、約160兆円)にも上ると言われています。世界の医療用医薬品市場の成長率は2017-2022年の年平均で7.1%の成長を続けており、2022-2028年の予測においても年平均で約6.1%の成長が見込まれています。1
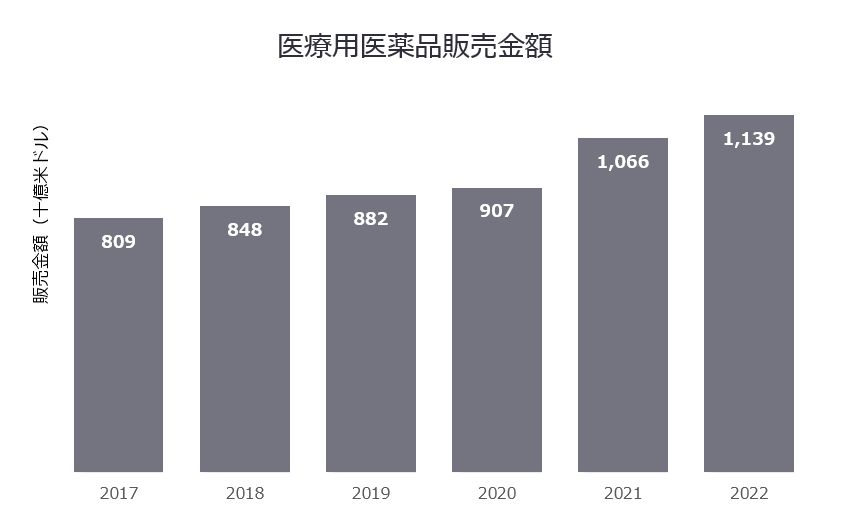
(単位:十億米ドル)
| 2017 | 2018 | 2019 |
2020 | 2021 | 2022 | |
| 医療用医薬品販売金額 | 809 |
848 |
882 | 907 | 1,066 | 1,139 |
画像1【世界の医薬品市場の推移】出典:Evaluate Pharma『WORLD PREVIEW 2022 Outlook to 2028:Patents and Pricing」Worldwide total prescription drug sales (2014-2028)』より執筆者作成
1 Evaluate Pharma『WORLD PREVIEW 2022 Outlook to 2028』 における予測
医薬品業界において最も大きな市場は米国で2022年度の医療用医薬品売上高は約5000億米ドルと世界全体の売上の4割強を占めています。OTCや医療機器を含む医薬品及び医療機器の市場を地域別に分割したものが、以下の円グラフとなります。
北米地域が46.5%、アジア太平洋地域が24.4%、西ヨーロッパ地域が16.6%の順で続いており、北米の市場が最も大きいことが分かります。また、アフリカ地域は1.4%と人口に比較して小さな市場であることが分かります。
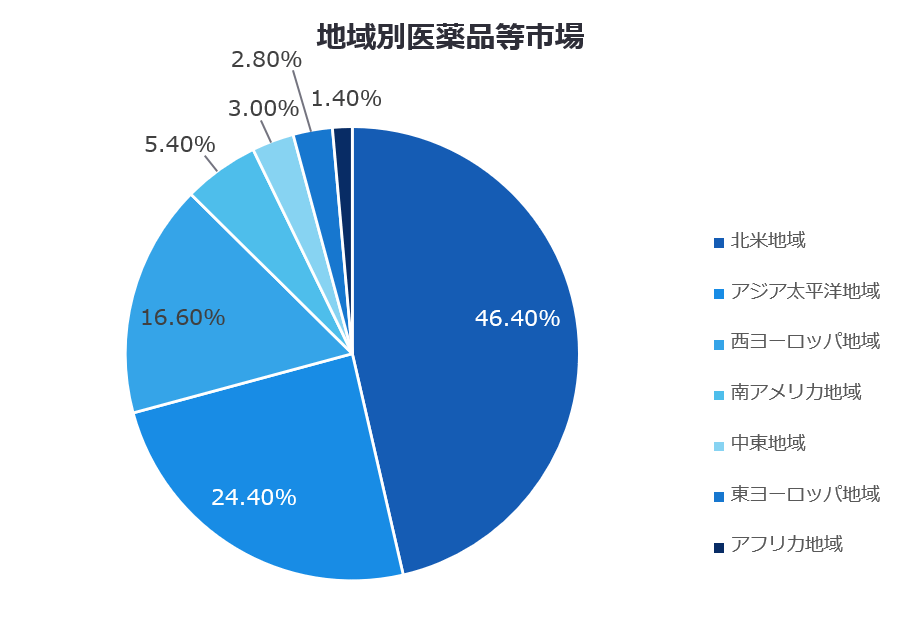
画像2【地域別医薬品等市場】出典:The Business Research Company「Pharmaceuticals Global Market Briefing 2023」2022年12月より執筆者作成
2017-2022年の年平均の成長率を見てみると、中東地域11.0%、南米地域8.4%、アジア太平洋地域7.1%の順で続いており、各地域の経済発展と一定の相関関係があることが推測されます。また、2022-2027年の予測成長率においても、中東地域、南米地域、アジア太平洋地域、アフリカ地域は7%を超える高い成長率が見込まれています。一方で、北米地域、ヨーロッパ西部地域は5%台の成長に留まっています。
図表2【地域別医薬品等市場成長率】
| 地域 | 成長率(%) 2017-2022 |
予測成長率(%) 2022-2027 |
| 北米地域 | 6.0 | 5.5 |
| アジア太平洋地域 | 7.1 | 7.8 |
| 西ヨーロッパ地域 | 5.5 | 5.5 |
| 南アメリカ地域 | 8.4 | 7.4 |
| 中東地域 | 11.0 | 8.0 |
| 東ヨーロッパ地域 | 4.8 | 6.4 |
| アフリカ地域 | 6.7 | 7.7 |
| 合計 | 6.4 | 6.3 |
出典:The Business Research Company「Pharmaceuticals Global Market Briefing 2023」2022年12月より執筆者作成
また、医療用医薬品市場には売上高が1,000億米ドルを超えるような巨大企業が存在しており、彼らはM&Aを積極的に行い、グローバルに展開しています。2022年時点での世界の製薬企業を売上高順に並べたものが以下の表です。
図表3【製薬企業売上高】各社公表資料より、執筆者が医療用医薬品業界の2022年度の売上高の上位を抽出
| No | 所在国 | 企業名 | 決算期 | 売上高 (百万米ドル) |
| 1 | アメリカ合衆国 | Pfizer Inc | 2022/12 | 100,330 |
| 2 | アメリカ合衆国 | Johnson & Johnson | 2022/12 | 94,943 |
| 3 | スイス | Roche Holding AG | 2022/12 | 66,310 |
| 4 | アメリカ合衆国 | Merck & Co Inc | 2022/12 | 59,283 |
| 5 | アメリカ合衆国 | AbbVie Inc | 2022/12 | 58,054 |
| 6 | ドイツ | Bayer AG | 2022/12 | 53,455 |
| 7 | スイス | Novartis AG | 2022/12 | 51,828 |
| 8 | フランス | Sanofi SA | 2022/12 | 47,819 |
| 9 | アメリカ合衆国 | Bristol-Myers Squibb Co | 2022/12 | 46,159 |
| 10 | イギリス | AstraZeneca PLC | 2022/12 | 44,351 |
| 11 | イギリス | GSK PLC | 2022/12 | 36,273 |
| 12 | 中国 | Shanghai Pharmaceuticals Holding Co Ltd | 2022/12 | 34,509 |
| 13 | 中国 | China Resources Pharmaceutical Group Ltd | 2022/12 | 32,450 |
| 14 | 日本 | 武田薬品工業 | 2023/03 | 29,785 |
| 15 | アメリカ合衆国 | Eli Lilly and Co | 2022/12 | 28,451 |
次に、日本市場に目を移すと、2021年度の医療用医薬品市場の規模は約11兆6千億円であり、2020年度に比較して若干増加したものの、10兆円強の水準を維持しています。日本では超高齢化社会の到来による医療用医薬品の処方増加に伴う社会保障費圧迫に対応するため、政府による薬価の引き下げや、後発医薬品の使用促進による医薬品の売上高の抑制を図っています。この点は後半の、「3-1. 薬価の形成プロセスと関連する規制」で詳しく説明します。
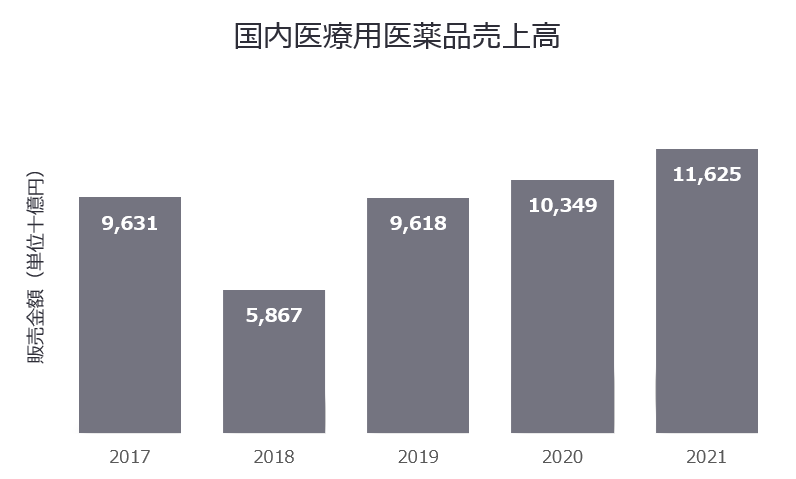
(単位:十億円)
| 2017 | 2018 | 2019 |
2020 | 2021 | |
| 医療用医薬品 | 9,631 | (※) 5.867 |
9,618 | 10,349 |
11,625 |
※ 2018年度は調査期間における新型コロナウイルス流行の影響により、大企業を含め回答数が少なく、実態と乖離している。
画像3【国内医療用医薬品売上高】令和3年度医薬品・医療機器産業実態調査より抜粋
なお、日本の製薬企業を売上高順で並べたものが以下の表です。
図表4【国内製薬企業売上高】各社公表資料より、執筆者が医療用医薬品業界の2022年の売上高の上位を抽出
| No | 企業名 | 決算期 | 売上高 (十億円) |
| 1 | 武田薬品工業 | 2023/3 | 4,027 |
| 2 | 大塚ホールディングス | 2022/12 | 1,737 |
| 3 | アステラス製薬 | 2023/3 | 1,518 |
| 4 | 第一三共 | 2023/3 | 1,278 |
| 5 | 中外製薬 | 2022/12 | 1,259 |
| 6 | エーザイ | 2023/3 | 744 |
| 7 | 住友ファーマ | 2023/3 | 555 |
| 8 | 小野薬品工業 | 2023/3 | 447 |
| 9 | 塩野義製薬 | 2023/3 | 426 |
| 10 | 協和キリン | 2022/12 | 398 |
参考文献・参考ウェブページ
厚生労働省HP www.mhlw.go.jp/index.html(2023年12月)
独立行政法人 医薬品医療機器総合機構HP www.pmda.go.jp/(2023年12月)
U.S. Food and Drug Administration www.fda.gov/(2023年12月)
European Medicines Agency www.ema.europa.eu/en/homepage(2023年12月)
Evaluate Pharma 『WORLD PREVIEW 2022 Outlook to 2028 : Patents and Pricing」Worldwide total prescription drug sales (2014-2028)』 (2022年10月)
The Business Research Company 『Pharmaceuticals Global Market Briefing 2023』 (2022年12月)
ライフサイエンス
- 第1回:ライフサイエンス業界の概要と動向(上) (2024.03.05)
- 第2回:ライフサイエンス業界の概要と動向(下) (2024.03.06)
- 第3回:新薬を中心とした医療用医薬品製造販売業の概要と会計処理の特徴 (2024.03.08)
- 第4回:一般用医薬品製造販売業の概要と会計処理の特徴 (2024.03.11)
- 第5回:ジェネリック医薬品(後発医薬品)を中心とした医療用医薬品製造販売業の概要と会計処理の特徴 (2024.03.13)
- 第6回:医薬品製造受託機関(CMO)・医薬品開発製造受託機関(CDMO)の概要と会計処理の特徴 (2024.03.14)
- 第7回:医療機器製造販売業の概要と会計処理の特徴 (2024.03.15)
- 第8回:医薬品卸売業の概要と会計処理の特徴 (2024.03.18)
- 第9回:バイオベンチャー企業のビジネスと財務諸表の特徴 (2024.03.25)
- 第10回:バイオベンチャー企業におけるライセンス契約の会計処理論点 (2024.03.26)
- 第11回:ライフサイエンス関連企業における不正・コンプライアンスリスクと最近の動向 (2024.03.27)
- 第12回:バイオベンチャー企業の株式上場における論点 (2024.03.28)
- 第13回:ライフサイエンス関連企業のサステナビリティ情報開示 (2024.04.02)




