CRC業務モニタリング・コンプライアンス態勢強化支援
EY Forensicsは、製薬会社(CRO)や医療機関自身とは独立した立場からモニタリングを実施することでCRC業務の実態を客観的に把握し、改善が必要なプロセスを洗い出します。SOP(Standard Operating Procedures)やマニュアルの更新支援に加え、リスクアプローチに基づくさらなるコンプライアンス態勢の強化に向けた改善提案により、近年社会から注目される臨床研究に係るリスク低減に向けたご支援をします。
臨床研究で増加するリスクとその影響
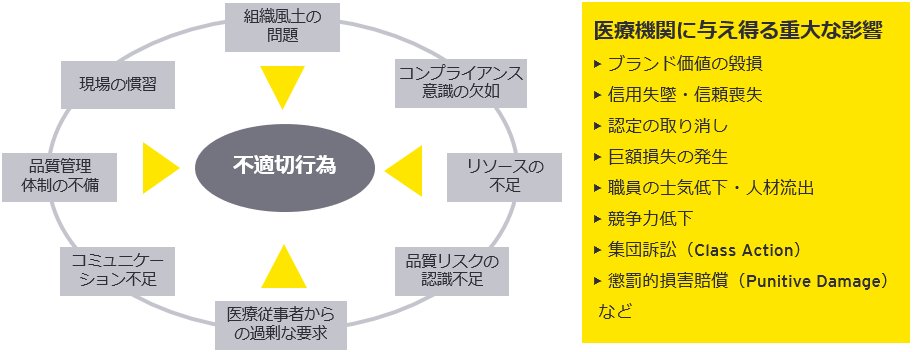
臨床研究データの改ざんやねつ造など、CRC(Clinical Research Coordinator)による不適切行為が相次いで発覚しています。臨床研究上の不適切行為は治験薬の承認申請取り下げや依頼者(製薬会社など)による損害賠償請求をもたらす可能性があるだけでなく、医療機関の信用や信頼、評判を大きく落としかねません。臨床研究法の施行やGCP(Good Clinical Practice)の改正を背景に、今や医療機関自らが品質を確保しなければならない時代となりました。
臨床研究の外部への業務委託が増加する中、委託者である医療機関がどのように管理監督責任を果たすのか、今そのあり方が問われています。
EY ForensicsによるCRC業務モニタリング・コンプライアンス態勢強化支援
医療機関が管理監督責任を果たすには、不適切行為が生じるリスクの効果的かつ効率的な管理に加え、小さな不正・ミスの発生時に適時適切な対応を取ることができるような仕組みの整備・運用や組織風土の醸成が必要不可欠です。
EY Forensicsは、医療機関のSOP(Standard Operating Procedures)やマニュアルなどを基に、CRC業務の実態を把握した上で改善が必要なプロセスを洗い出し、さらなるコンプライアンス態勢の強化に向けた改善提案により、臨床研究に係るリスクの低減に向けたご支援をします。
調査項目例
CRC業務モニタリング・コンプライアンス態勢強化支援の流れ
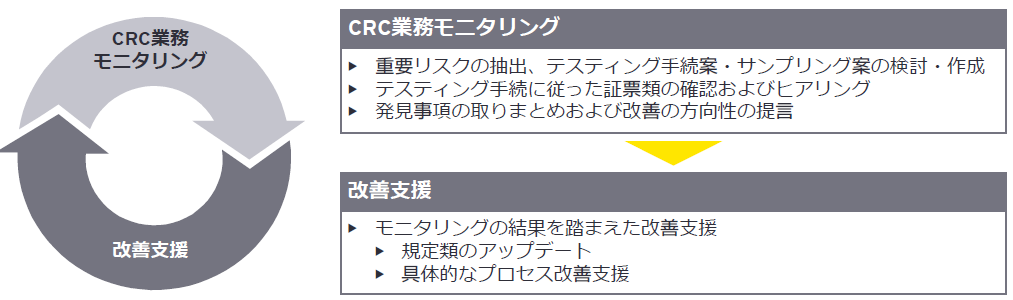
オプションとして以下のご支援も可能です
- 貴社モニタリングご担当者へ向けたナレッジトランスファー
病院主体によるモニタリングを実施可能にするためのナレッジトランスファーセッション実施 - CRC向け研修支援
EYによる実態調査結果の伝達、および不正行為(不適切行為)に係る講義の提供
※一部サービスについては、独立性の事前確認が必要となります。独立性上の観点から、業務を一部制限させていただく、またはお引き受けできない可能性がある旨、あらかじめご了承ください。
EY Forensicsによる支援の特徴
知見と経験を生かした不正行為(不適切行為)の観点から分析
過去の不正調査やコンプライアンスモニタリングを通じて検出した具体的な事例や手口などを参考に、さまざまなリスクシナリオを織り込んだ、効果的かつ効率的なサンプルテストを実現します。
第三者に「見られている」というけん制効果
製薬会社や院内部署ではなく、第三者であるEYが実施するため、客観的な目線によるモニタリングや改善提案が可能です。また、不適切行為へのけん制効果により、リスク管理の実効性を高めることが期待できます。
ヘルスケア/ライフサイエンスセクターへの高品質なサービス
EYは長年にわたり、国立大学法人、グループ医療法人などへ、会計監査のみならず非監査業務においても高品質なサービスを提供しています。国内外のネットワークと緊密に連携しながら、豊富な経験を持つプロフェッショナルがサポートします。
チーム
お問い合わせ
より詳しい情報をご希望の方はご連絡ください。


